
Suyun Elektrolizi Nasıl Yapılır?
Suyun elektrolizi, elektrik akımı kullanarak suyu hidrojen ve oksijen gazlarına ayırma işlemidir. Bu süreç, enerji üretimi ve çevre dostu uygulamalar için önemli bir yöntemdir. Elektroliz, hidrojen üretimi ve yenilenebilir enerji sistemleri gibi alanlarda geniş kullanım alanlarına sahiptir.
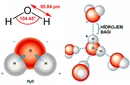
Suyun elektrolizi, suyun elektrik akımı kullanılarak hidrojen ve oksijen gazlarına ayrıştırılması işlemidir. Bu süreç, enerji üretimi, kimyasal sentez ve çevre dostu enerji kaynaklarının geliştirilmesi gibi birçok alanda önemli uygulamalara sahiptir. Bu makalede, suyun elektrolizinin temel prensipleri, kullanılan yöntemler ve uygulama alanları ele alınacaktır. Elektroliz Nedir?Elektroliz, bir elektrolit çözeltisi içerisinde elektrik akımının geçirilmesiyle kimyasal bileşiklerin ayrıştırılması veya bileşenlerinin yeniden düzenlenmesi işlemidir. Su, iyi bir elektrolit olmasa da, içerisine belirli tuzlar veya asitler eklenerek elektroliz işlemi gerçekleştirilebilir. Suyun elektrolizinde, su molekülleri (H₂O), hidrojen (H₂) ve oksijen (O₂) gazlarına ayrılır. Elektroliz İşleminin Temel Prensipleri Suyun elektrolizinin temel prensipleri şunlardır:
Elektroliz Yöntemleri Suyun elektrolizi çeşitli yöntemlerle gerçekleştirilebilir:
Uygulama Alanları Suyun elektrolizi, birçok alanda kullanılmaktadır:
Sonuç Suyun elektrolizi, enerji üretimi ve çevre koruma açısından büyük bir potansiyele sahip bir süreçtir. Gelişen teknoloji ile birlikte elektroliz yöntemlerinin verimliliği artmakta ve hidrojen üretimi daha sürdürülebilir hale gelmektedir. Bu süreç, gelecekte temiz enerji sistemlerinin temel bileşenlerinden biri olma yolunda ilerlemektedir. |
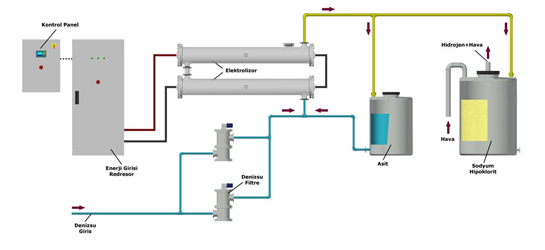



























Anot ve kanot ile üretilen oksijen ve hidrojen birbirinden nasıl ayrıştırılır
Oksijen ve Hidrojenin Ayrıştırılması
Anot ve kanot, elektroliz işlemi sırasında kullanılan elektrotlardır. Bu işlem, suyun elektroliz edilmesiyle oksijen ve hidrojen gazlarının ayrıştırılmasını sağlar.
Elektroliz Süreci
Elektroliz işlemi, suyun elektrik akımı ile parçalanmasıdır. Bu süreçte, suyun bileşenleri olan hidrojen ve oksijen ayrı gazlar olarak ortaya çıkar. Anot, pozitif elektrot olup oksijen gazı üretirken, kanot negatif elektrottur ve hidrojen gazı üretir.
Ayrıştırma Mekanizması
1. Elektrik Akımı Uygulama: Suya uygulanan elektrik akımı, su moleküllerini parçalayarak hidrojen ve oksijen iyonlarını oluşturur.
2. Gazların Toplanması: Anot üzerinde oluşan oksijen gazı, yüzeyde birikirken, kanot üzerinde oluşan hidrojen gazı da aynı şekilde birikir. Bu gazlar, elektrotların üzerindeki tüpler veya kaplar aracılığıyla toplanabilir.
3. Gazların Ayrıştırılması: Toplanan gazlar, ayrı kaplarda biriktirilerek birbirinden ayrışır. Oksijen ve hidrojen gazları, farklı özelliklere sahip olduklarından, bu aşamada kolayca ayrılabilir.
Bu yöntem, suyun bileşenlerine ayrıştırılmasında etkili bir yöntemdir ve laboratuvar ortamlarında yaygın olarak kullanılmaktadır.
bu elektroliz sonucunda çıkan oksijeni insanlar tüketebilir mi
Evet, elektroliz sonucunda elde edilen oksijen insanlar tarafından tüketilebilir. Elektroliz, suyu oksijen ve hidrojen gazlarına ayırır ve bu süreçte elde edilen oksijen, solunabilir saflıkta olur. Ancak, pratik uygulamalarda güvenlik ve saflık kontrolü önemlidir.