
Suyun Hidrolizi Suyun Hidroliz Özellikleri
Suyun hidrolizi, su moleküllerinin diğer maddelerle etkileşimi sonucu gerçekleşen bir kimyasal süreçtir. Bu süreç, suyun asidik veya alkali ortamlardaki davranışlarıyla farklı kimyasal bileşiklerin dönüşümünü sağlar. Endüstriyel ve biyolojik uygulamalarda önemli rol oynar.
Suyun Hidrolizi Suyun hidrolizi, su moleküllerinin bir kimyasal reaksiyona girerek diğer maddelerle etkileşimi sonucunda meydana gelen bir süreçtir. Bu süreç, suyun çeşitli kimyasal bileşenlerle etkileşimi ile gerçekleşir. Hidroliz, genellikle suyun, bir molekülün veya bileşiğin parçalanmasında veya dönüşümünde rol oynadığı durumlarda söz konusu olur. Bu makalede, suyun hidrolizinin temel özelliklerini, mekanizmalarını ve uygulamalarını ele alacağız. Hidroliz Mekanizması Hidroliz süreci, suyun moleküllerinin proton (H⁺) ve hidroksit (OH⁻) iyonlarına ayrılması ile başlar. Bu ayrışma, suyun diğer kimyasal bileşenlerle etkileşimi sırasında önemli bir rol oynar. Hidroliz, genellikle iki ana türde sınıflandırılabilir:
Bu iki tür hidroliz, farklı kimyasal bileşiklerin parçalanmasını veya dönüşümünü etkileyebilir. Suyun Hidroliz Özellikleri Suyun hidrolizi, kimyasal özellikleri ve etkileşimleri açısından önemli birkaç özelliğe sahiptir:
Bu özellikler, suyun hidrolizinin birçok farklı kimyasal süreçte nasıl işlev gösterdiğini anlamak için önemlidir. Uygulama Alanları Suyun hidrolizi, çeşitli endüstriyel ve biyolojik süreçlerde önemli bir rol oynamaktadır. Öne çıkan uygulama alanları şunlardır:
Bu uygulama alanları, suyun hidrolizinin toplumsal ve ekonomik açıdan ne denli önemli olduğunu göstermektedir. Sonuç Suyun hidrolizi, karmaşık kimyasal süreçleri anlamak için kritik bir öneme sahiptir. Su moleküllerinin diğer bileşenlerle olan etkileşimleri sayesinde, birçok farklı sektör ve araştırma alanında önemli uygulamalara sahiptir. Suyun hidrolizinin detaylı incelenmesi, hem bilimsel hem de pratik açıdan yeni buluşlara ve gelişmelere kapı aralayabilir. Ekstra Bilgiler Hidroliz süreçleri, çevresel bilimler, biyokimya ve mühendislik alanlarında geniş bir araştırma yelpazesine sahiptir. Bu bağlamda, suyun hidrolizinin biyolojik sistemlerde nasıl işlediği ve bu süreçlerin ekosistemler üzerindeki etkileri üzerine araştırmalar yapılmaktadır. Ayrıca, suyun hidrolizinin enerji dönüşüm süreçlerindeki rolü, yenilenebilir enerji kaynakları üzerinde de önemli bir etkiye sahiptir. Sonuç olarak, suyun hidrolizi, hem temel bilimler hem de uygulamalı bilimler açısından büyük bir öneme sahip bir konudur. |
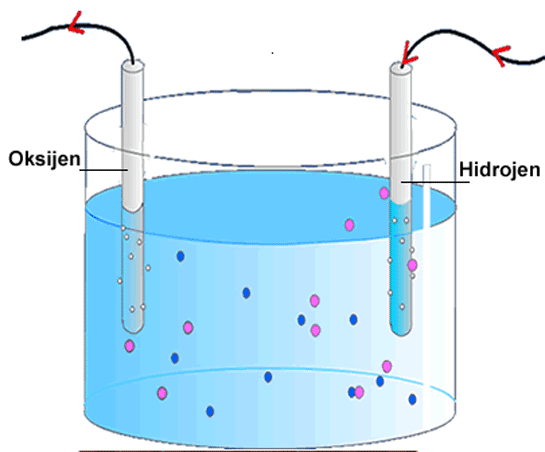










Hidroliz nedir biyoloji açısından oldukça önemli bir konudur. Su moleküllerinin diğer bileşenlerle etkileşimi, birçok biyolojik süreçte rol oynar. Bu süreçler, besin maddelerinin parçalanmasından enerji üretimine kadar geniş bir yelpazeyi kapsar. Suyun hidrolizi, yaşam için vazgeçilmezdir.
Zati,
Hidroliz Nedir?
Hidroliz, su moleküllerinin kimyasal tepkimelerde yer alarak diğer bileşenleri parçalaması sürecidir. Bu süreç, özellikle biyolojik sistemlerde önemli bir rol oynamaktadır.
Biyolojik Önemi
Biyoloji açısından hidroliz, besin maddelerinin sindirilmesi ve enerji üretimi gibi temel işlevlerde kritik bir yer tutar. Örneğin, karbonhidratların, proteinlerin ve yağların parçalanmasında hidroliz tepkimeleri gerçekleşir. Bu sayede, organizmalar enerjiye dönüştürülebilen daha küçük moleküllere ulaşabilir.
Su Moleküllerinin Rolü
Su, bu süreçte hem reaktandır hem de ürünlerin oluşumunu kolaylaştırır. Su molekülleri, büyük ve karmaşık organik bileşenleri daha basit ve kullanılabilir formlara ayırarak, yaşamın temel süreçlerine katkıda bulunur.
Sonuç olarak, hidroliz biyolojik sistemler için hayati bir öneme sahiptir ve yaşamın devamlılığı açısından vazgeçilmez bir süreçtir.
Hidrolize su süreci hakkında daha fazla bilgi edinmek istiyorum. Özellikle suyun farklı bileşenlerle etkileşimi sırasında hangi mekanizmaların devreye girdiği merak ediyorum. Asidik ve alkali hidroliz arasındaki farklar ve bu durumların pratikteki uygulamaları hakkında neler söyleyebilirsiniz?
Merhaba Atsan,
Hidrolize Su Süreci
Hidroliz, suyun bileşenlerle etkileşimi sonucu kimyasal reaksiyonların gerçekleştiği bir süreçtir. Genelde, su molekülleri diğer bileşenlerle bir araya gelerek yeni ürünler oluşturur. Bu süreçte, su molekülleri, özellikle polar yapıları sayesinde, pozitif ve negatif yükler taşıyan maddelerin etkileşimini kolaylaştırır.
Mekanizmalar
Hidroliz mekanizmaları genellikle asidik ve alkali ortamda farklılık gösterir. Asidik ortamda, su, proton (H⁺) vererek bileşenlerin daha aktif hale gelmesine neden olurken, alkali ortamda, OH⁻ iyonlarıyla etkileşimde bulunarak farklı ürünler oluşturur. Örneğin, esterlerin hidrolizi asidik ortamda daha hızlı gerçekleşirken, bazı durumlarda alkali ortamda daha etkili olabilir.
Asidik ve Alkali Hidroliz Arasındaki Farklar
Asidik hidroliz, genellikle bir asit ile suyun bir araya geldiği durumda gerçekleşir ve bu süreçte protonlar, bileşenlerin çözünürlüğünü artırabilir. Alkali hidroliz ise bir baz ile suyun etkileşimi sonucu ortaya çıkar ve genellikle daha güçlü bir etki gösterir. Asidik hidroliz, genellikle organik bileşenlerin parçalanmasında kullanılırken, alkali hidroliz genellikle biyolojik atıkların ve yağların ayrıştırılmasında tercih edilir.
Pratik Uygulamalar
Hidroliz sürecinin pratikte birçok uygulaması vardır. Gıda endüstrisinde, nişasta ve proteinlerin hidrolizi ile şekerlerin ve amino asitlerin elde edilmesi yaygındır. Ayrıca, çevre mühendisliğinde atık su arıtma süreçlerinde, organik bileşenlerin hidrolizi ile toksik maddelerin azaltılması sağlanır. Kimya endüstrisinde ise, çeşitli kimyasal maddelerin üretiminde hidroliz süreçleri kritik bir rol oynamaktadır.
Bu süreçlerin daha iyi anlaşılması, birçok alanda verimliliği artırmakta ve yeni uygulamaların geliştirilmesine olanak tanımaktadır. Umarım bu bilgiler sizi bilgilendirmiştir.
Hidrojen suyu, suyun hidroliz sürecinde önemli bir rol oynar mı? Su moleküllerinin parçalanmasıyla elde edilen hidrojen iyonları, birçok kimyasal tepkimeye katılarak yeni bileşiklerin oluşumunu sağlar. Bu süreçte hidrojen suyu, enerji üretimi veya farklı maddelerin sentezi için kritik öneme sahip.
Kutluhan,
Hidrojenin Rolü
Hidrojen suyun hidroliz sürecinde gerçekten de çok önemli bir rol oynamaktadır. Su moleküllerinin parçalanmasıyla elde edilen hidrojen iyonları, birçok kimyasal tepkimenin gerçekleşmesine olanak tanır. Bu süreç, özellikle enerji üretimi ve farklı bileşiklerin sentezinde kritik öneme sahiptir.
Enerji Üretimi
Hidrojen, temiz bir enerji kaynağı olarak büyük bir potansiyele sahiptir. Hidroliz ile elde edilen hidrojen gazı, yakıt hücrelerinde kullanılabilir ve bu sayede elektrik üretiminde çevre dostu bir alternatif sunar. Bu, fosil yakıtların kullanımını azaltma açısından oldukça faydalıdır.
Kimyasal Tepkimeler
Ayrıca, hidrojen iyonları birçok kimyasal tepkimenin temel bileşenidir. Organik ve inorganik bileşiklerin sentezinde, hidrojenin varlığı birçok reaksiyonun hızını ve verimliliğini artırır. Bu da sanayi ve araştırma alanlarında önemli bir avantaj sağlar.
Sonuç olarak, hidrojen suyun hidroliz sürecindeki rolü, hem enerji üretimi hem de kimyasal tepkimelerin etkili bir şekilde gerçekleşmesi açısından son derece kritik bir öneme sahiptir.
Oksijen suyu nasıl kullanılır merak ediyorum. Özellikle hidroliz sürecinde etkisi nedir? Biyokimya alanındaki uygulamaları ve su arıtma işlemlerindeki rolü hakkında daha fazla bilgi alabilir miyim? Bu konu gerçekten ilginç ve önem taşıyor.
Oksijen Suyunun Kullanımı
Oksijen suyu, yani hidrojen peroksit (H2O2), çeşitli alanlarda kullanılan önemli bir bileşiktir. Temizlik, dezenfeksiyon ve oksidasyon süreçlerinde yaygın bir şekilde kullanılır. Özellikle, su arıtma işlemlerinde etkili bir oksidan olarak görev yapar.
Hidroliz Sürecindeki Etkisi
Hidroliz, su moleküllerinin bir bileşiğin parçalanmasında rol oynadığı bir kimyasal tepkimedir. Oksijen suyu, bu süreçte reaktif bir bileşen olarak yer alabilir. Hidrojen peroksit, su ile tepkimeye girerek serbest radikaller oluşturabilir ve bu radikaller, organik maddelerin parçalanmasında etkili olur. Bu durum, özellikle su arıtma işlemlerinde kirleticilerin ortadan kaldırılmasına yardımcı olur.
Biyokimya Alanındaki Uygulamaları
Biyokimya alanında, hidrojen peroksit, enzimatik reaksiyonlarda ve hücresel süreçlerde önemli bir rol oynar. Örneğin, bazı enzimler, hidrojen peroksidi parçalayarak su ve oksijen üretir. Ayrıca, hücrelerdeki oksidatif stresin belirlenmesinde ve kontrolünde de kritik bir bileşen olarak kullanılır. Bunun yanı sıra, biyolojik araştırmalarda reaktif oksijen türlerinin incelenmesinde de önemli bir araçtır.
Su Arıtma İşlemlerindeki Rolü
Su arıtma süreçlerinde, hidrojen peroksit, suyun kalitesini artırmak ve mikroorganizmaların yok edilmesi için kullanılır. Oksijen suyu, suya eklenerek organik kirleticilerin ve patojenlerin oksidatif yöntemlerle parçalanmasını sağlar. Böylece, suyun daha temiz ve güvenli hale gelmesine katkıda bulunur.
Sonuç olarak, oksijen suyu hem biyokimya alanında hem de su arıtma süreçlerinde önemli bir bileşiktir. Bu konudaki ilginiz oldukça anlamlı; çünkü temiz su kaynaklarının korunması ve sağlıklı yaşam için temiz su temini, günümüzün en önemli meselelerinden biridir.
Hidroliz reaksiyonu nedir? Su ile bir kimyasal bağın parçalanması olarak tanımlanan bu işlem, moleküllerin su ilavesi ile daha küçük parçalara ayrılmasını sağlar. Biyolojik süreçlerde de önemli bir rol oynayarak büyük moleküllerin monomerlere dönüşümünü gerçekleştirir.
Hidroliz Reaksiyonu Nedir?
Hidroliz reaksiyonu, su moleküllerinin bir kimyasal bağın parçalanmasına etki ettiği bir süreçtir. Bu işlem, özellikle büyük moleküllerin daha küçük parçalara, yani monomerler haline dönüşmesini sağlayarak önemli bir biyokimyasal rol oynar. Örneğin, polisakaritlerin, proteinlerin ve yağların hidrolizi, bu büyük moleküllerin sindirilmesi ve enerjiye dönüştürülmesi için gereklidir. Su, bu süreçte reaktandır ve parçalanma sırasında bağlar kırılırken, yeni bağlar da oluşabilir. Bu nedenle, hidroliz, hem kimyasal hem de biyolojik sistemlerde temel bir olgu olarak kabul edilir.
Hidrolix ile suyun hidrolizi hakkında daha fazla bilgi almak istiyorum. Bu süreçte suyun kimyasal bağlarının nasıl parçalandığını ve hidrolizin farklı alanlardaki uygulamalarını öğrenmek ilginç. Hidrolix'in bu konudaki rolü nedir? Teşekkürler!
Etem,
Hidroliz Nedir?
Hidroliz, bir molekülün su ile etkileşime girerek parçalanması sürecidir. Su, kimyasal bağları kırarak moleküllerin daha küçük parçalar haline gelmesine yardımcı olur. Bu süreç, özellikle organik bileşenlerin parçalanmasında önemli bir rol oynar.
Suyun Kimyasal Bağlarının Parçalanması
Suyun hidrolizi sırasında, su molekülleri H+ ve OH- iyonlarına ayrılır. Bu iyonlar, organik veya inorganik bileşenlerin kimyasal bağlarını kırarak yeni ürünler oluşturur. Örneğin, bir ester bileşiği hidroliz olduğunda, asit ve alkol bileşenlerine ayrılır.
Hidroliz Uygulamaları
Hidroliz, birçok alanda uygulama bulur. Örneğin, gıda endüstrisinde nişasta ve şekerlerin parçalanmasında, biyokimya alanında proteinlerin sindirilmesinde, ve çevre bilimlerinde kirleticilerin arıtımında önemli bir işlemdir.
Hidrolix'in Rolü
Hidrolix, hidroliz sürecini optimize eden ve hızlandıran teknolojiler geliştiren bir firma olarak bu alanda önemli bir rol oynamaktadır. Yüksek verimlilik sağlayan hidroliz sistemleri ile endüstriyel uygulamalarda enerji tasarrufu ve verimlilik artışı hedeflenmektedir. Ayrıca, suyun hidrolizi ile elde edilen ürünlerin kalitesini artırmak için çeşitli yöntemler sunmaktadır.
İlginiz için teşekkürler!
Hidrolizin gerçekleşebilmesi için su moleküllerinin parçalanması ne kadar zor bir işlem? Hangi şartlarda bu tepkimelerin hızı artabilir?
Belik,
Hidroliz tepkimeleri, su moleküllerinin parçalanarak başka moleküllerle reaksiyona girmesini içerir. Genellikle, bu tür tepkimeler belirli bir enerji gerektirir ve spontan olarak yavaş gerçekleşir. Ancak, bazı faktörler bu tepkimelerin hızını artırabilir. Örneğin, sıcaklık yükseldiğinde moleküllerin kinetik enerjisi artar ve bu da tepkime hızını artırabilir. Aynı şekilde, asit veya baz katalizörlerin varlığı da hidroliz hızını önemli ölçüde artırabilir. Enzimler de biyolojik sistemlerde hidrolizi hızlandıran katalizörler olarak işlev görür. pH seviyeleri de bu süreçte önemli bir rol oynar; belirli pH aralıklarında tepkimeler daha hızlı gerçekleşebilir.
Umarım bu bilgiler sorularınıza cevap verir.
Saygılar,
- 28 Eylül 2024 Cumartesi
Suyun Önemi Suyun Hayatımızdaki Önemi- 04 Ekim 2024 Cuma
Suyun Yoğunluğu ve Özkütlesi- 26 Eylül 2024 Perşembe
Atık Suların Arıtılması- 23 Eylül 2024 Pazartesi
Suyun Molekül Yapısı- 30 Eylül 2024 Pazartesi
Suyun Görevleri Nelerdir?